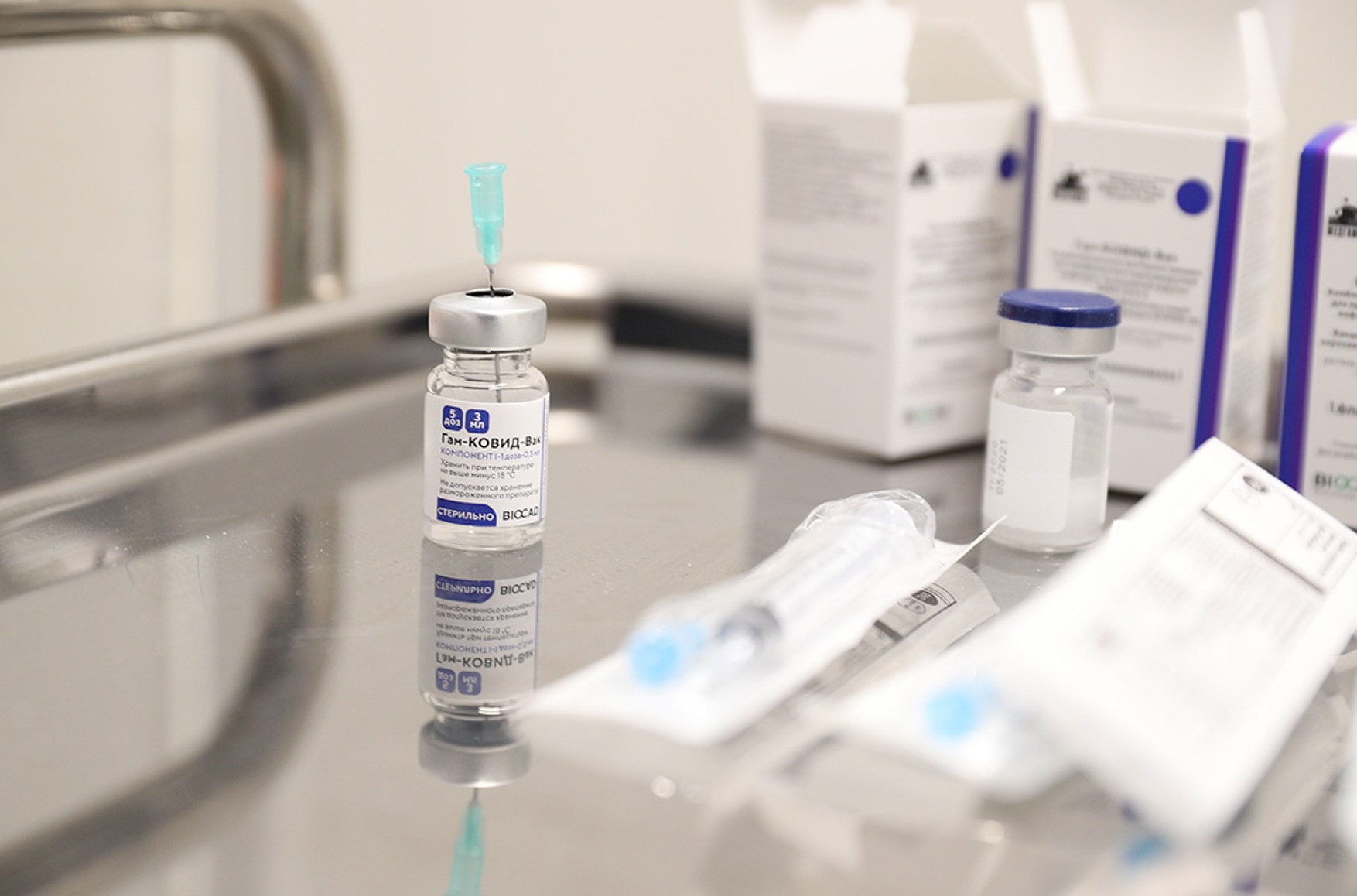
Для оцінки ефективності російської вакцини від коронавируса «Супутник V» і її реєстрації на території ЄС необхідні додаткові дані від розробника. Про це заявив глава відділу по вакцинації і боротьби з інфекціями Європейського агентства лікарських засобів (EMA) Марко Кавалери, передає Reuters.
«Що стосується вакцин” Супутник V “і [китайської] Sinovac, обговорення цих препаратів з виробниками було конструктивним, але нам потрібно [отримати] більше даних, перш ніж продовжити роботу за їхньою оцінкою», – сказав він. За його словами, у зв'язку з відсутністю додаткових даних про виробництво, безпеки та ефективності «Супутника» говорити про терміни його реєстрації передчасно.
Сьогодні вакцина «Супутник V» схвалена для застосування більш ніж в 60 країнах. У січні РФПИ подав заявку на реєстрацію препарату в Європейське медичне агентство (EMA). Експертизу «Супутника» почали в березні. Як писав Reuters, регулятор повинен був винести рішення по препарату ще в травні, проте терміни довелося зрушити до кінця року через те, що розробник – Центр ім. Гамалії – пропустив крайній термін подачі даних про випробування. РФПИ це заперечував.
Інше джерело агентства, близький до EMA, повідомив, що до початку літа регулятор не отримав майже ніяких виробничих даних по вакцині, а надані клінічні відомості були неповними. Йдеться в тому числі про звіти про побічні ефекти. Гендиректор РФПИ Кирило Дмитрієв говорив, що фахівці EMA в ході процедури експертизи «Супутника» не висловили критичних зауважень ні до якості проведених випробувань, ні до самого виробництва.









