Кількість виявлених випадків коронавіруса в світі досягло близько 6,5 млн, загиблих — вже понад 385 тисяч, але ніяких доведено ефективних методів лікування, так само як і вакцини, як і раніше немає. 2 червня ВООЗ оновив список розробляються вакцин, в який, крім понад 130 інших, потрапили 10 проектів з Росії. Венчурний інвестор у сфері біотехнології та фармацевтики Антон Гопка аналізує як використовуються проти COVID препарати, так і перспективні розробки.
Через п’ять місяців після перших повідомлень про появу нового вірусу можна робити обережні висновки, які надії на способи лікування виправдовуються, а які виявилися помилковими.
Результати стрес-тесту систем охорони здоров’я довели головна теза глобального рейтингу медичної безпеки: ні одна країна в світі повною мірою не готова до епідемії чи пандемії. Зазвичай під цим мають на увазі брак ліжок, персоналу або апаратів ШВЛ. На практиці з’ясувалося, що саме «ліжка» можна легко розгорнути. У січні в Ухані за лічені дні побудували модульну лікарні на 1000 ліжок. У Нью-Йорку лікарні розгорнули прямо в Центральному парку. А в Москві гігантський «госпіталь» розмістили у торговому центрі «Крокус Експо». Питання не в ліжках, а в тому, як вони обладнані, яка діагностика використовується, які препарати і медустройства. Тобто якщо і робити резерв, то не простоюють ліжок, а терапевтичних і превентивних засобів фармацевтики і медичного обладнання.
Початковим етапом боротьби з поширенням епідемії стали нефармацевтические дії: посилені заходи особистої гігієни, обов’язкове носіння масок, закриття шкіл та університетів, заборона на проведення масових заходів і припинення міжнародного сполучення з вогнищами епідемії. В останні тижні вийшли публікації по ефективності цих заходів та економічних наслідків від ВООЗ, Світового банку, а також ретроспективний аналіз з Китаю. Масштаб, тривалість і потенційні «побічні» ефекти цих заходів, як і раніше, спірні, але, в будь-якому випадку, їх головна мета — виграти час для системи охорони здоров’я.
Соціальна реклама засобів особистого захисту в Зімбабве
За препаратів само регулярно з’являються суперечливі дані. У дискусію включилися всі, включаючи людей, далеких від медицини і біотехнологій. Це нормально, оскільки питання медицини одномоментно торкнулися всіх. Тим не менш від лідерів думок очікувалася особлива відповідальність і стриманість у висловлюваннях. Проте їхні повідомлення в Twitter з передчасними заявами про «доведеної ефективності тих чи інших препаратів призводили до різкого дефіциту для тих, кому вони дійсно потрібні. Такі повідомлення в соцмережах і недавні гучні прес-релізи впливають на громадську думку, але точно не підвищують безпеку і ефективність розроблюваних ліків і вакцин.
Як відомо, розробка нового препарату займає приблизно 7-10 років. Ймовірність успіху проходження всіх етапів, від лабораторних розробок до ринку, — менше 5%. У зв’язку з такими тривалими термінами в умовах пандемії можливо тільки репозиціонувати вже відомі препарати, довівши їх ефективність проти нового коронавіруса. Важливо розуміти, що ймовірність успіху перепозиционированного старого препарату проти COVID-19 вкрай низька. Але ліки потрібні вже сьогодні, з цієї причини в хід йдуть всі можливості. Тому потік новин з вивчення ефективності та безпеки препаратів проти COVID-19 нагадує серіал з масою сюжетних ліній, дійових осіб і перипетій.
Найгучніший препарат
В середині березня з’явилися перші повідомлення про ефективність препарату гидроксихлорохина, схваленого у США більше 70 років тому і використовується проти ревматоїдного артриту та малярії. Дональд Трамп тоді назвав його «одним з найбільших проривів в історії медицини», потім була рекомендація від Ілона Маска. Препарат миттєво випарувався з аптечних полиць. The New York Times виявила в трастах президента США наявність невеликих часток великої фармацевтичної компанії Sanofi, що виробляє гідроксихлорохін. Але це сміховинне звинувачення: препарат вийшов з-під патентного захисту, не є важливим для Sanofi, і його виробляють більше десятка компаній.
Дональд Трамп рекламує гідроксихлорохін
22 травня в медичному журналі The Lancet вийшла наукова публікація за результатами аналізу клінічних даних понад 96 тисяч пацієнтів, 14 тисяч з яких брали хлорохины. Ученим не вдалося виявити ознаки ефективності препаратів: навпаки, виявилися гірші клінічні наслідки у зв’язку з відомими побічними ефектами. У зв’язку з цією публікацією на минулого тижня ВООЗ призупинив клінічне дослідження по гидроксихлорохину, так само вчинили країни Європейського союзу і Великобританія, яка за підтримки Bill & Melinda Gates Foundation запустила дослідження по 40 000 медпрацівникам буквально за кілька днів до цього. З минулого тижня Франція, Італія і Бельгія припинили подальше застосування хлорохіну проти COVID-19, за винятком клінічних досліджень. Але вже в середу ВООЗ, вивчивши дані, продовжив клінічне дослідження і набір пацієнтів.
Трамп переконаний, що критика хлорохіну — це атака на його політичну кампанію. Він як і раніше наполягає на ефективності ліків і нібито приймає його в профілактичних цілях, хоча опубліковане в середу дослідження про профілактику захворювання в медичному журналі NEJM встановило, що препарат не запобігає захворювання, якщо почати його застосовувати відразу після взаємодії з інфікованими. Ентоні Фаучі, головний інфекціоніст США, в інтерв’ю CNN минулого тижня висловився з приводу препарату цілком однозначно: «Наукові дані досить очевидні — гідроксихлорохін не показує ефективності проти COVID-19, але призводить до ризиків для серцево-судинної системи».
Вчора вийшов новий несподіваний епізод серіалу про гідроксихлорохін: з’ясувалося, що та сама публікація шановного рецензованого медичного журналу The Lancet, яка призвела до припинення клінічних досліджень в глобальному масштабі, виявилася заснована на даних, наданих американською компанією Surgisphere, не вселяє довіри.
22 травня в журналі The Lancet вийшла стаття, автори якої проаналізували дані про 96 тисяч пацієнтів, яких лікували гидроксихлорохином, і прийшли до висновку, що він істотно збільшує смертність. За підсумками цієї публікації ВООЗ призупинила свої поточні клінічні дослідження гидроксихлорохина.
Проте вчені і журналісти засумнівалися в даних статті, журналісти The Guardian встановили, що цифри по Австралії не відповідають дійсності. Після листування з засновником компанії Surgisphere Сапаном Десаї журналісти вирішили дізнатися, що це за компанія. У Surgisphere 11 співробітників, велика частина з яких почала працювати кілька місяців тому і не має досвіду в науковій сфері. Науковий редактор виявився письменником-фантастом, серед інших працівників виявилися адміністратор публічних заходів (event hostess), маркетолог і порномодель. Лікарні, з якими пов’язувалися журналісти, заявили, що не знають таку компанію ніяких відомостей їй не передавали. Кілька сотень вчених підписали відкритий лист з вимогою провести розслідування.
The Lancet публічно визнав сумнівність наведених даних, хоча це не скасовує і всіх підозр з приводу хлорохіну.
Препарати прямої дії
Інший, поки більш успішний препарат, — ремдесивир від компанії Gilead. Він розробляється вже 10 років: спочатку його використовували проти гепатиту С (невдало), потім проти Еболи (провалився в минулому році), тепер же — проти нової коронавирусной інфекції.
В епоху пандемії його швидко схвалили за прискореною процедурою термінового дозволу на застосування (Emergency Use Authorisation) на підставі даних клінічного дослідження другої фази. Минулого тижня був опублікований аналіз попередніх даних третьої (останньої) фази клінічних досліджень. Єдина важлива новина — ефективність препарату в цілому однакова при п’ятиденному і десятиденному курсі застосування. Тобто системі охорони здоров’я можна «зекономити» і скоротити обсяг закуповуваного ліки.
На відміну від неспецифічного гидроксихлорохина препарат володіє прямим механізмом дії: він порушує роботу РНК-полімерази — «копіювальної машини» РКН-вірусів. За наявними даними, препарат скорочує період одужання в середньому з 15 днів до 11. Це істотно для системи охорони здоров’я в момент перевантаження, але не є лікуванням для пацієнтів. У будь-якому випадку це, ймовірно, кращий засіб, що є на даний момент.
Лабораторія Gilead Sciences в Каліфорнії
Є ще один препарат з аналогічним механізмом дії. 1 червня Моз повідомив про реєстрацію першого російського препарату проти нового коронавіруса: ним став Авифавир на підставі попередніх даних клінічних досліджень, проведених в рекордні терміни. Розробка проведена Російським фондом прямих інвестицій (РФПІ) та групою компаній «Хімрар». Цей противірусний препарат був винайдений в Японії компанією Fujifilm і схвалений у 2014 році для лікування нових штамів грипу.
Прем’єр-міністр Сіндзо Абе висловлював надію, що препарат буде схвалений для лікування COVID-19 у травні цього року на основі попередніх даних, але минулого тижня уряд відклав затвердження препарату ще мінімум на місяць для одержання переконливих даних про його ефективність. Крім того, важливо мати на увазі, що препарат має ризиками тератогенної дії (порушення ембріонального розвитку) і протипоказаний вагітним.
Препарат Авифавир увійшов в оновлені тимчасові клінічні рекомендації з лікування нової коронавирусной інфекції, які були опубліковані 3 червня. Інший російської новинкою в списку можливих до призначення препаратів стало ліки Артлегиа (олокизумаб), раніше зареєстроване за показником «ревматоїдний артрит». Права на розробку та комерціалізацію цього препарату були куплені російською компанією Р-Фарм в 2013 році у бельгійської UCB.
Зараз препарат проходить третю фазу міжнародних клінічних досліджень за основним показанням і розглядається по показанню COVID-19 в США. Механізм дії препарату — інгібування інтерлейкіну-6, який викликає цитокіновий шторм, надлишкову реакцію імунної системи. Препарати з таким механізмом дії вже активно використовуються при терапії COVID-19 у всьому світі, в тому числі найбільш відомий — Actemra (тоцилизумаб) від компанії Roche/Genentech.
Крім цих препаратів, є сотні інших репозиционированных і оригінальних — практично кожна поважаюча себе биотехкомпания змогла виявити придатність своєї розробки до COVID-19 у зв’язку з багатогранністю захворювання. Але остаточним вирішенням проблеми COVID-19 стане вакцина.
Вакцини
2 червня ВООЗ оновив свій реєстр розробляються в світі вакцин. У списку виявилося 133 розробки, з яких по десяти вже ведуться клінічні дослідження. Що особливо вражає — у списку вже десять проектів з Росії: до двом кандидатам від BIOCAD (в тому числі спільно з Санкт-Петербурзьким Інститутом експериментальної медицини) та Санкт-Петербурзького НДІ вакцин і сироваток — додалися шість від сибірського «Вектора» і одна розробка від МДУ. З урахуванням заявлених Тетяною Голікової 47 розробок вакцин в Росії, ймовірно, список ВООЗ ще буде поповнюватися. Також, за словами віце-прем’єра, на розробку вакцини від COVID-19 та тест-систем для діагностики захворювання виділено 3,1 млрд рублів (близько $40 млн).
Процес розробки вакцини, як правило, ще довше, ніж у препаратів, оскільки вона буде широко застосовуватися і до десятків мільйонів здорових людей, тому вимоги до них ще суворіше. Вибірка досліджуваних кількісно повинна відповідати масового використання вакцини. У рамках клінічних досліджень перевіряють імунну відповідь на ті чи інші дії. Цей імунну відповідь виробляється не моментально і важливо відстежити, як довго вона зберігається, і чи є які-небудь, потенційно відстрочені побічні ефекти. Все це — біологічні процеси, які неможливо кратно прискорити. Все одно що просити вагітних жінок народити не за 9 місяців, а за місяць.
Вакцини можна розділити умовно на три групи: розроблені на основі самого вірусу (ослабленого або інактивованого), його білків (антигенів або виросом) і генетичного коду (векторні і ДНК/РНК-вакцини). Перші вакцини ґрунтувалися на ослабленому вірус — тобто такий штам вірусу, який пристосований до тварин, а не до людини, але може викликати у щепленого повноцінний імунну відповідь. Оскільки в даному випадку вірус «живий», потрібні великі клінічні дослідження, підтверджують його безпеку. Інактивовані віруси — це оброблені віруси, які не здатні в принципі заражати клітини, тому вони безпечніше ослаблених, але можуть викликати занадто слабка імунна відповідь.
Білкові вакцини засновані на штучно отриманих окремих вірусних білках-антигенах. Вони безпечні, але дороги у виробництві і не завжди дають стійкий імунітет, тому що окремий білок може відрізнятись за формою від білка, вбудованого в оболонку вірусу. Також розробляються вакцини на основі «порожніх» вірусних частинок з поверхневих білків, але без вірусної ДНК або РНК всередині.
Самий «просунутий» тип вакцини — це вакцини, засновані на фрагментах геному вірусу, що кодують вірусні білки-антигени. Такі вакцини доставляють в клітку генетичний код вірусу і клітини перетворюють людину на фабрики по виробництву антигенів, які викликають імунну відповідь. Однак ці вакцини ще жодного разу не були схвалені для застосування в людях. Головна їхня перевага — це можливість стрімкої розробки нових вакцин, оскільки в даному випадку можна просто поміняти код згідно з новим вірусом або новою мутацією.
Але в умовах пандемії запущена гонка на розробку вакцини в немислимі раніше терміни — до осені, дослідження ведуться паралельно, безпека відстежується протягом декількох місяців, а не років. У США запущений проект «Warp Speed» («Надзвукова швидкість»), який, згідно інформації від 3 червня, підтримає, імовірно, 5-7 найбільш перспективних і досвідчених розробок, включаючи великі фармкомпанії Johnson & Johnson, Merck, Pfizer і AstraZeneca в колаборації з Оксфордським університетом, а також американську биотехкомпанию Moderna. Управління перспективних біомедичних досліджень і розробок Моз США (BARDA) вже виділило $500 млн для J&J і $1,2 млрд для розробки AstraZeneca з Оксфордським університетом. Ймовірно, будуть виділені ще кошти.
Найбільш цікава розробка у компанії Moderna, оскільки це інноваційна платформа для розробки вакцин на основі генетичного коду вірусу — його РНК. Moderna стала першим у світі розробником, підготували новий кандидат вакцини — протягом 40 днів після публікації геному вірусу. Також компанія першою почала клінічні дослідження на людях. Moderna поки не розкриває попередні дані і тільки ділиться успіхами у форматі гучних прес-релізів.
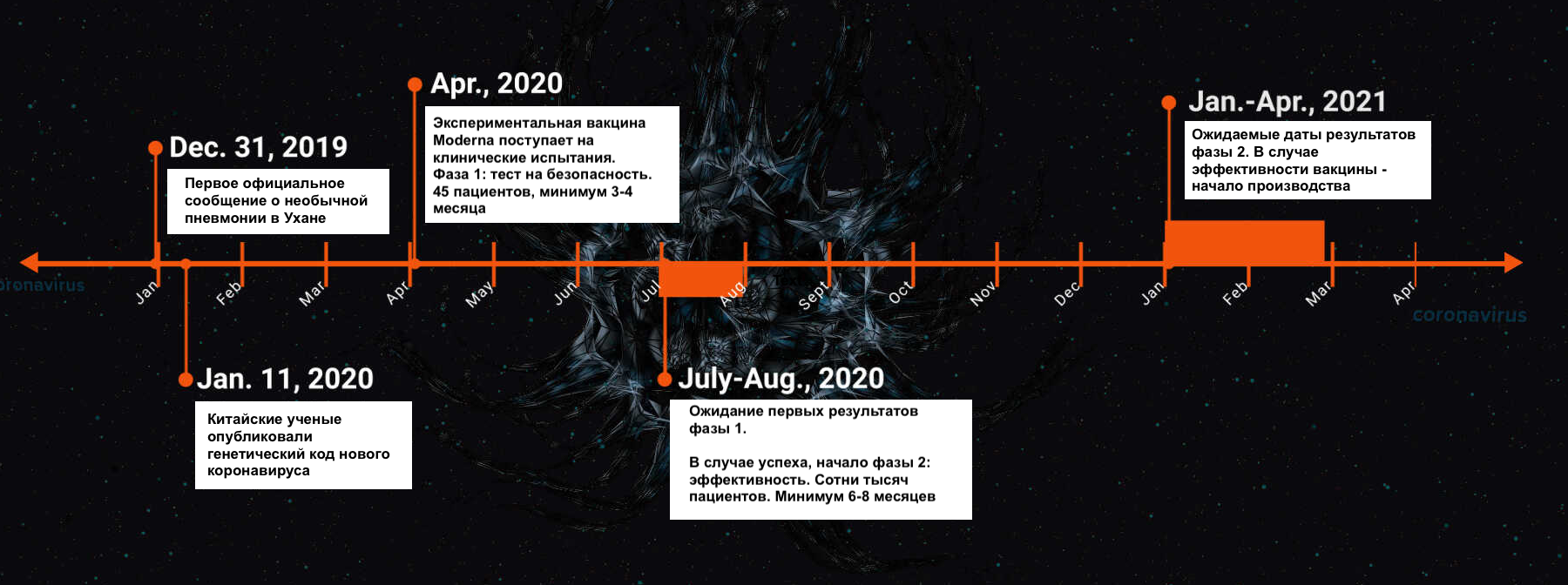
Хроніка розробки вакцини. Джерело: National Institute of Allergy and Infectious Diseases
Розкрита лише інформація про перших восьми добровольцях, але судити про ефективність або безпеки поки рано. В учасників клінічного дослідження імовірно виробилися антитіла в тому обсязі, в якому їх виявляли у людей, що перехворіли COVID-19. Але цього недостатньо, щоб судити про клінічної цінності вакцини: захищає цей титр антитіл від зараження, як і раніше невідомо. Згідно з протоколом, стан учасників дослідження потрібно відстежувати ще протягом року. При цьому головний медичний директор Moderna заявив в прес-релізі, що чекає на остаточні дані по ефективності на початку січня 2021, «якщо все піде добре».
Остаточні дані щодо ефективності Moderna очікуються в січні 2021 року
Ці заяви призвели акції компанії до піку (зростання — понад 300% з початку року). Кілька керівників почали продавати свої акції на десятки мільйонів доларів. Складно припустити, що фінансовий директор компанії, колишній банкір Goldman Sachs, і головний медичний директор Moderna могли б порушити якісь необхідні процедури для таких дій, але вони продали свої активи на загальну суму близько $30 млн, і це привернуло увагу регулятора ринку цінних паперів США у зв’язку з потенційним «маніпулюванням ринку» та гучними заявами із дуже попередніми даними.
Ще одну вакцину на основі платформи, аналогічної Moderna, розробляє раніше згадана російська компанія BIOCAD. Робота знаходиться на стадії доклінічних досліджень. В цілому ситуація, що склалася, дає Росії можливість продемонструвати вміння у розробці фармпрепаратів і вакцин. Російські фармкомпанії з глобальними амбіціями прагнуть максимально відповідати міжнародним стандартам біоетики та проведення клінічних досліджень, що стає в нинішніх умовах одним з головних конкурентних переваг розробок з неосновних фармринків.